Мы используем файлы cookie и аналогичные технологии для правильной работы этого сайта, а также для анализа и оптимизации трафика просмотра. Продолжая просмотр сайта, вы соглашаетесь на использование таких файлов cookie.
Продукты SonoScape получили знак CE в соответствии с регламентом EU-MDR.
1970-01-01 08:33:44
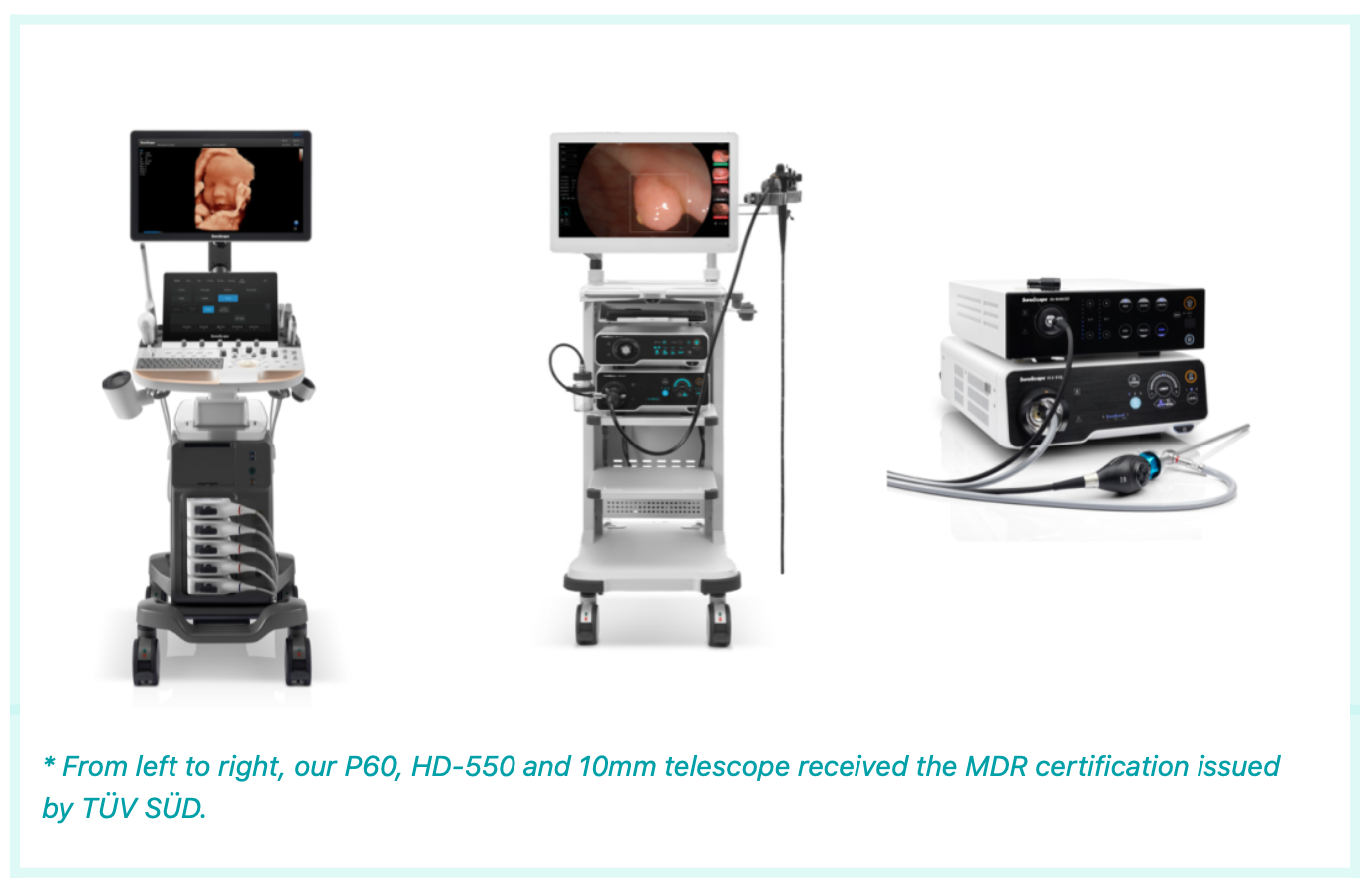
Благодаря своему стремлению к инновациям SonoScape может предложить комплексный и постоянно расширяющийся портфель технологий визуализации, включая решения для УЗИ, эндоскопии и малоинвазивной хирургии. Это укрепляет ее роль поставщика решений для улучшения диагностических и лечебных возможностей медицинских учреждений.
В середине апреля этого года система HD-550 получила одобрение FDA 510(k), благодаря чему SonoScape смогла предложить поставщикам медицинских услуг в США новые решения с более ярким и четким изображением. Одобрение CE-MDR придало SonoScape значительный импульс к развитию международной торговли. "Введя более строгие требования соответствия, MDR подняли планку для наших медицинских устройств, продаваемых в ЕС, — сказал Стивен Хе, директор по продажам подразделения эндоскопии. — Получение маркировки CE в рамках MDR обещает нам высокий уровень защиты пациентов и нашу долгосрочную поддержку сообщества эндоскопистов в ЕС".
"Очень интересно наблюдать, как SonoScape достигает поставленных целей и получает паспорт ЕС для своих систем для УЗИ и эндоскопии, — прокомментировал Дэвид Ляо, директор по продажам подразделения ультразвуковой диагностики. — Мы очень рады, что дошли до этого этапа, и с нетерпением ждем возможности отправиться в ЕС, чтобы предложить им новый способ эффективной ультразвуковой диагностики".